Anhand zweier klinischer Fälle werden im Folgenden grundlegende Prinzipien der Diagnostik, Therapie und Sekundärprophylaxe von venösen Thromboembolien (VTE) dargestellt.
Kasuistik 1: tiefe Beinvenenthrombose
Eine 35-jährige Frau wird mit einer Beinschwellung rechts an der Ambulanz vorstellig. Bei einer Körpergröße von 162cm wiegt sie 61kg. Ihr Blutdruck ist mit 120/80mmHg normal. Anamnestisch liegt eine Sprunggelenksverletzung 2 Wochen vor dem Ambulanzbesuch vor, die dazu geführt hat, dass die Patientin sich seither nur wenig bewegt hat. Klinisch ließ sich eine Zunahme des Umfangs des rechten Unterschenkels um 3,2cm im Vergleich zum linken feststellen, was die Diagnose Beinvenenthrombose nahelegt.
In den ESC-Guidelines wird empfohlen, die Vortest-Wahrscheinlichkeit standardisiert zu erheben.1 Der am weitesten verbreitete Score zur Ermittlung der klinischen Wahrscheinlichkeit einer VTE ist der Wells-Score, in dem Faktoren wie aktive Tumorerkrankung, Immobilisation, Schmerz und Schwellung oder frühere tiefe Venenthrombosen (TVT) erhoben werden.2 Für jeden Faktor wird 1 Punkt vergeben und bei einem Resultat von 2 oder mehr Punkten ist die Wahrscheinlichkeit für eine TVT hoch.
Im vorliegenden Fall der 35-jährigen Patientin ergab der Wells-Score 5 Punkte, was für eine hohe TVT-Wahrscheinlichkeit im Vortest spricht und keine weitere Labordiagnostik vor der Bildgebung erforderlich macht. Für die bildgebende Diagnostik der TVT ist die Kompressionssonografie die Methode der Wahl. Damit konnte die Diagnose bei der Patientin gesichert werden.
Antikoagulation bei VTE
Da es sich in diesem Fall um eine provozierte VTE handelt – die Patientin hat sich während der vergangenen zwei Wochen wenig bewegt, ist vorwiegend gesessen oder gelegen –, wird eine Antikoagulation für drei Monate empfohlen.1 Weitere provozierende Faktoren können rezente Operationen, Traumata, Schwangerschaft, Wochenbett oder die Einnahme weiblicher Hormone sein.
In den internationalen Guidelines wird bei VTE die Antikoagulation mit einem direkten bzw. neuen oralen Antikoagulans (NOAK) empfohlen.1, 3 Derzeit stehen mit Rivaroxaban (Xarelto®), Apixaban (Eliquis®) und Edoxaban (Lixiana®) drei direkte Faktor-Xa-Inhibitoren und mit Dabigatran (Pradaxa®) ein direkter Faktor- IIa(Thrombin)-Inhibitor zur Verfügung. Für alle vier NOAK konnte in den jeweiligen Zulassungsstudien im Vergleich zu Vitamin-K-Antagonisten (VKA) eine Nicht- Unterlegenheit in Bezug auf die Verhinderung weiterer thrombotischer Ereignisse bei zumindest gleichem Blutungsrisiko nachgewiesen werden.4 Für zwei Substanzen, Apixaban und, bei Patienten mit Lungenembolie, Rivaroxaban, ergaben die Zulassungsstudien eine im Vergleich zu LMWH/VKA signifikante Reduktion von schweren Blutungsereignissen.5, 6
Unterschiede zwischen den Präparaten bestehen hinsichtlich des Behandlungsschemas. Während die Therapie mit Apixaban und Rivaroxaban direkt begonnen wird (wobei in der Anfangsphase eine höhere Dosis zum Einsatz kommt), ist bei Edoxaban und Dabigatran ein „Lead-in“ mit niedermolekularem Heparin für mindestens 5 Tage erforderlich.
Je nach NOAK kann eine individuelle Dosisreduktion notwendig sein; hier sind insbesondere auch Unterschiede zwischen den Indikationen zu beachten. Angaben zur Dosisreduktion sind den jeweils aktuellen Fachinformationen zu entnehmen.
Die Patientin mit der diagnostizierten Beinvenenthrombose erhielt für 1 Woche Apixaban 10mg zweimal täglich und anschließend für drei Monate Apixaban 5mg zweimal täglich. Da das Risiko bei einem transienten Ereignis, das behoben wurde, sehr gering ist, wurde die Therapie nach drei Monaten beendet. Die Patientin ist bis heute beschwerdefrei und hat kein weiteres thromboembolisches Ereignis erlitten.
Kasuistik 2: Pulmonalembolie
In der Ambulanz wird ein 62-jähriger Mann mit Dyspnoe und Thoraxschmerz vorstellig. Bei einer Körpergröße von 178cm wiegt er 84kg. Sein Blutdruck beträgt 130/90mmHg und der letzte vier Wochen alte Laborbefund zeigt keine Auffälligkeiten. In der Anamnese wurde eine Pulmonalembolie (PE) vor vier Jahren erhoben, wobei kein auslösender Faktor identifiziert werden konnte. Sonst lagen keine augenscheinlichen kardiovaskulären Risikofaktoren vor.
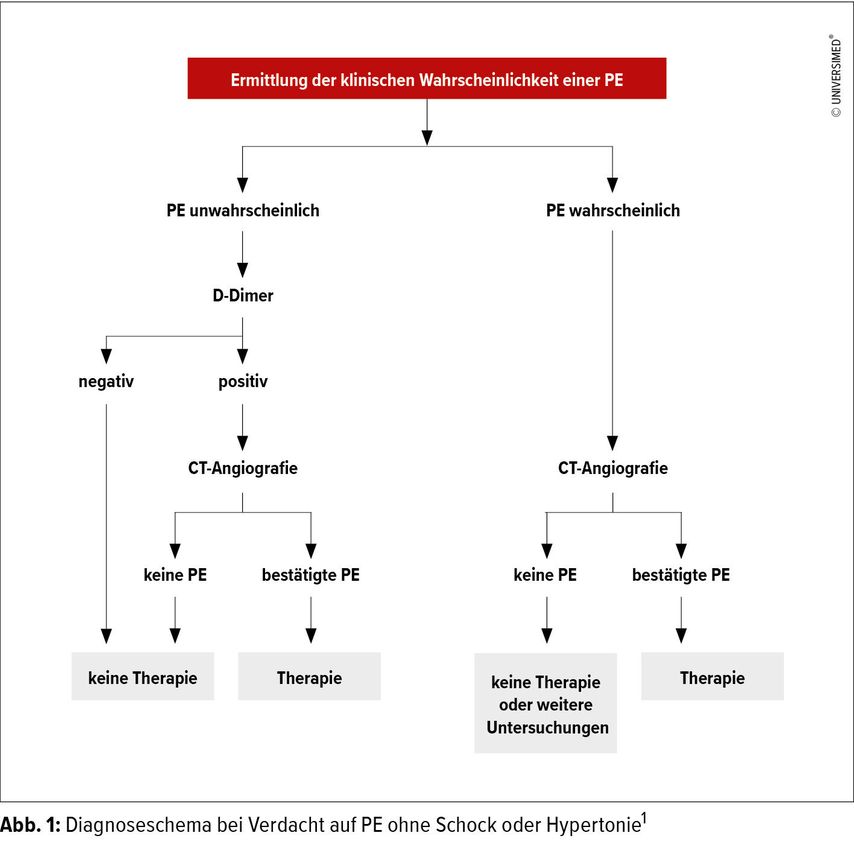
Im EKG zeigten sich eine prominente S-Zacke in Ableitung I sowie eine prominente Q-Zacke in Ableitung III. Dieser sogenannte SIQIII-Typ lässt bereits an eine PE denken. Auffallend war darüber hinaus eine Sinus-Tachykardie mit einer Frequenz von 110/min. Für die PE existiert ein spezifischer Wells-Score, der sich etwas von jenem für die VTE unterscheidet. So fließen in dieser Version Faktoren wie frühere PE oder TVT, Tachykardie, chirurgische Eingriffe oder Hämoptysen ein.1 Ab einem Wert von 2 Punkten ist laut der vereinfachten Version des Wells-Scores eine PE wahrscheinlich. Der Patient erreichte 3 Punkte. In den ESC-Guidelines wird ein konkretes Diagnoseschema bei Verdacht auf PE ohne Schock oder Hypotonie empfohlen (Abb. 1). Da beim vorliegenden Patienten der Vortest eine hohe Wahrscheinlichkeit für eine PE ergab, wurde sofort ein Thorax- CT angefertigt, in dem eine beidseitige, massive zentrale PE diagnostiziert wurde. Zur Evaluierung des Mortalitätsrisikos wird in den ESC-Guidelines die Ermittlung des vereinfachten PESI-Scores (sPESI) empfohlen, in dem Parameter wie Alter, Geschlecht, das Vorliegen eines Malignoms, Herzinsuffizienz, chronische Lungenerkrankung, Pulsfrequenz ≥110/min, Hypotonie sowie eine Sauerstoffsättigung <90% jeweils 1 Punkt ergeben. Hat der Patient in diesem Score 0 Punkte, so ist das 30-Tage-Mortalitätsrisiko mit 1% gering, bei 1 oder mehr Punkten liegt das 30-Tage-Mortalitätsrisiko bei 10,9%.7
Blutungsrisiko beachten
Laut ESC-Guidelines ist bei einem Patienten mit PE primär das Risiko abzuschätzen.1 Ist der Patient im Schock oder hypoton (<90mmHg systolisch), hat er ein hohes Mortalitätsrisiko und eine primäre Reperfusion ist indiziert. Bei geringem Risiko (sPESI = 0) sind theoretisch eine Antikoagulation und eine ambulante Behandlung möglich. In Österreich werden Patienten mit PE jedoch auch bei geringem Risiko stationär aufgenommen. Bei intermediärem Risiko sind Antikoagulation, Hospitalisierung sowie initiale Überwachung indiziert.
Dieser Patient hat ein intermediäres Risiko (sPESI = 1) und bereits eine unprovozierte PE in der Anamnese, weshalb sein Rezidivrisiko über 5 Jahre bei 25 bis 30% liegt.8 Hier empfiehlt sich eine dauerhafte Antikoagulation.
Bei langfristiger Antikoagulation ist das Blutungsrisiko unter der Therapie zu beachten. In der AMPLIFY-EXTENSION-Studie konnte gezeigt werden, dass im Endpunkt „VTE-Rezidiv oder VTE-bedingter Tod“ nach 12 Monaten unter Apixaban 2x tgl. 2,5mg oder 2x tgl. 5mg im Vergleich zu Placebo eine signifikante Reduktion erzielt werden konnte (beide Dosierungen Apixaban 1,7% vs. Placebo 8,8%; p<0,001).9 Die Raten an großen oder klinisch relevanten Blutungen im Studienarm mit Apixaban 2x tgl. 2,5mg waren mit jenen in der Placebogruppe vergleichbar. Daraus leitet sich die Empfehlung in der Fachinformation ab, für die Langzeitantikoagulation Apixaban in einer Dosierung von 2x 2,5mg täglich einzusetzen.
Aufgrund des hohen Rezidivrisikos des Patienten und der sich daraus ergebenden Notwendigkeit für eine Dauertherapie wurde der Patient auf Apixaban eingestellt. Laut Therapieschema erhielt er Apixaban 10mg zweimal täglich für 7 Tage und ab dem 8. Tag 5mg zweimal täglich für 6 Monate. Danach wurde die Apixaban- Dosis auf zweimal täglich 2,5mg reduziert. Der Patient ist bis heute rezidivfrei und hatte auch kein relevantes Blutungsereignis.
Literatur
Konstantinides SV et al.: 2014 ESC Guidelines on the diagnosis and management of acute pulmonary embolism: the Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC). Eur Heart J 2014; 35(43): 3033-69, 3069a-3069k
Wells PS et al.: Does this patient have deep vein thrombosis? JAMA 2006; 295(2): 199-207
Kearon C et al.: Antithrombotic therapy for VTE disease: CHEST Guideline and Expert Panel Report. Chest 2016; 149(2): 315-52
Beyer-Westendorf J, Ageno W: Benefit-risk profile of non-vitamin K antagonist oral anticoagulants in the management of venous thromboembolism. Thromb Haemost 2015; 113(2): 231-46
Agnelli G et al.: Oral apixaban for the treatment of acute venous thromboembolism. N Engl J Med 2013; 369(9): 799-808
Büller HR et al.: Oral rivaroxaban for the treatment of symptomatic pulmonary embolism. N Engl J Med 2012; 366(14): 1287-97
Jiménez D et al: Simplification of the pulmonary embolism severity index for prognostication in patients with acute symptomatic pulmonary embolism. Arch Intern Med 2010; 170(15): 1383-9
Kyrle PA et al.: The long-term recurrence risk of patients with unprovoked venous thromboembolism: an observational cohort study. J Thromb Haemost 2016; 14(12): 2402-9
Agnelli G et al.: Apixaban for extended treatment of venous thromboembolism. N Engl J Med 2013; 368(8): 699-708